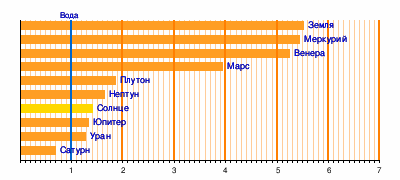
Плотность и удельный вес металлов и их сплавов
Содержание:
- Взаимодействие кислот с металлами
- Параметры никеля
- Плотность некоторых пород древесины
- Классификация стали
- Удельный вес металла. Таблица плотности металлов и сплавов
- Технические показатели сплавов металлов
- Металлы и их плотность
- Альтернативная классификация
- Свойства
- Пластичность:
- Особенности никеля и его сплавов
- Физические свойства металлов
- Сферы применения сплавов меди
- Подведем итоги
Взаимодействие кислот с металлами
С кислотами металлы реагируют по-разному. Металлы, стоящие в электрохимическом ряду активности металлов (ЭРАМ) до водорода, взаимодействуют практически со всеми кислотами.
Происходит реакция замещения, которая также является окислительно-восстановительной:
- Mg+2HCl=MgCl2+H2↑{\displaystyle {\mathsf {Mg+2HCl=MgCl_{2}+H_{2}\uparrow }}}
- 2Al+2H3PO4=2AlPO4+3H2↑{\displaystyle {\mathsf {2Al+2H_{3}PO_{4}=2AlPO_{4}+3H_{2}\uparrow }}}
Взаимодействие концентрированной серной кислоты H2SO4 с металлами
Окисляющие кислоты могут взаимодействовать и с металлами, стоящими в ЭРАМ после водорода:
- Cu+2H2SO4=CuSO4+SO2↑+2H2O{\displaystyle {\mathsf {Cu+2H_{2}SO_{4}=CuSO_{4}+SO_{2}\uparrow +2H_{2}O}}}
Сильно разбавленная кислота реагирует с металлом по классической схеме:
- Mg+H2SO4=MgSO4+H2↑{\displaystyle {\mathsf {Mg+H_{2}SO_{4}=MgSO_{4}+H_{2}\uparrow }}}
При увеличении концентрации кислоты образуются различные продукты:
- Mg+2H2SO4=MgSO4+SO2↑+2H2O{\displaystyle {\mathsf {Mg+2H_{2}SO_{4}=MgSO_{4}+SO_{2}\uparrow +2H_{2}O}}}
- 3Mg+4H2SO4=3MgSO4+S↓+4H2O{\displaystyle {\mathsf {3Mg+4H_{2}SO_{4}=3MgSO_{4}+S\downarrow +4H_{2}O}}}
- 4Mg+5H2SO4=4MgSO4+H2S↑+4H2O{\displaystyle {\mathsf {4Mg+5H_{2}SO_{4}=4MgSO_{4}+H_{2}S\uparrow +4H_{2}O}}}
Реакции для азотной кислоты (HNO3)
Продукты взаимодействия железа с HNO3 разной концентрации
- Cu+4HNO3(60%)=Cu(NO3)2+2NO2↑+2H2O{\displaystyle {\mathsf {Cu+4HNO_{3}(60\%)=Cu(NO_{3})_{2}+2NO_{2}\uparrow +2H_{2}O}}}
- 3Cu+8HNO3(30%)=3Cu(NO3)2+2NO↑+4H2O{\displaystyle {\mathsf {3Cu+8HNO_{3}(30\%)=3Cu(NO_{3})_{2}+2NO\uparrow +4H_{2}O}}}
При взаимодействии с активными металлами вариантов реакций ещё больше:
- Zn+4HNO3(60%)=Zn(NO3)2+2NO2↑+2H2O{\displaystyle {\mathsf {Zn+4HNO_{3}(60\%)=Zn(NO_{3})_{2}+2NO_{2}\uparrow +2H_{2}O}}}
- 3Zn+8HNO3(30%)=3Zn(NO3)2+2NO↑+4H2O{\displaystyle {\mathsf {3Zn+8HNO_{3}(30\%)=3Zn(NO_{3})_{2}+2NO\uparrow +4H_{2}O}}}
- 4Zn+10HNO3(20%)=4Zn(NO3)2+N2O↑+5H2O{\displaystyle {\mathsf {4Zn+10HNO_{3}(20\%)=4Zn(NO_{3})_{2}+N_{2}O\uparrow +5H_{2}O}}}
- 5Zn+12HNO3(10%)=5Zn(NO3)2+N2↑+6H2O{\displaystyle {\mathsf {5Zn+12HNO_{3}(10\%)=5Zn(NO_{3})_{2}+N_{2}\uparrow +6H_{2}O}}}
- 4Zn+10HNO3(3%)=4Zn(NO3)2+NH4NO3+3H2O{\displaystyle {\mathsf {4Zn+10HNO_{3}(3\%)=4Zn(NO_{3})_{2}+NH_{4}NO_{3}+3H_{2}O}}}
Легирование
Легирование — это введение в расплав дополнительных элементов, модифицирующих механические, физические и химические свойства основного материала.
Параметры никеля
Никель – это металл со свойственным ему серебристо-белым цветом. При температуре 1453 °C переходит в жидкое состояние, а кипит при 2732 °C. Никель пластичен, легко поддается обработке под воздействием давления.
Химическое свойство никеля характеризуется способностью образовывать соединения с разной степенью окисления. В естественных условиях на поверхности металла возникает тонкая пленка из оксида.
Металл обладает высоким показателем устойчивости к коррозии. Никель не реагирует с рядом концентрированных кислот и щелочей, но активно растворяется в разбавленной азотной кислоте.
 Вступая в химические реакции, никель образует летучие металлы и растворимые/нерастворимые соли
Вступая в химические реакции, никель образует летучие металлы и растворимые/нерастворимые соли
С никелем не вступают в реакцию:
- инертные газы;
- литий;
- калий;
- натрий;
- цезий;
- рубидий;
- стронций;
- барий;
- иридий;
- цезий.
С углеродным соединением никель образует карбонил — летучий переходный металл, используемый в процессе получения материалов высокого класса чистоты. Порошок никеля способен самовоспламеняться при соприкосновении с воздухом с образованием оксидов.
Никель продуцирует ряд растворимых и нерастворимых солей. Например, раствор сульфата металла придает жидкости зеленую окраску. Нерастворимые соли обычно имеют насыщенный желтый цвет.
Плотность некоторых пород древесины
Плотность древесины, г/см³
| Бальса | 0,15 | Пихта сибирская | 0,39 |
| Секвойя вечнозелёная | 0,41 | Ель | 0,45 |
| Ива | 0,46 | Ольха | 0,49 |
| Осина | 0,51 | Сосна | 0,52 |
| Липа | 0,53 | Конский каштан | 0,56 |
| Каштан съедобный | 0,59 | Кипарис | 0,60 |
| Черёмуха | 0,61 | Лещина | 0,63 |
| Грецкий орех | 0,64 | Берёза | 0,65 |
| Вишня | 0,66 | Вяз гладкий | 0,66 |
| Лиственница | 0,66 | Клён полевой | 0,67 |
| Тиковое дерево | 0,67 | Бук | 0,68 |
| Груша | 0,69 | Дуб | 0,69 |
| Свитения (Махагони) | 0,70 | Платан | 0,70 |
| Жостер (крушина) | 0,71 | Тис | 0,75 |
| Ясень | 0,75 | Слива | 0,80 |
| Сирень | 0,80 | Боярышник | 0,80 |
| Пекан (кария) | 0,83 | Сандаловое дерево | 0,90 |
| Самшит | 0,96 | Эбеновое дерево | 1,08 |
| Квебрахо | 1,21 | Бакаут | 1,28 |
| Пробка | 0,20 |
Классификация стали
В зависимости от доли неметаллических примесей, определяемой методом выплавки данной марки, стальные сплавы разделяют на:
- особо высококачественные;
- высококачественные;
- обыкновенного качества.
По химическому составу сплавы также разделяют на легированные и углеродистые.
Углеродистые стали
Используются преимущественно для производства сварных конструкций и содержит от 0,25 до 2,14 процента углерода. Внутри группы они далее разделяются на подгруппы, и также по процентной доле углерода:
- высокоуглеродистые (0,6-2,14);
- среднеуглеродистые (0,3-0,55);
- низкоуглеродистые (ниже 0,25).
В качестве присадок в них также входят кремний и марганец.Кроме полезных, вводимых целенаправленно присадок в сплаве могут содержаться и вредные примеси, отрицательно влияющие на ее физико- химические свойства:
- фосфор снижает пластичность при нагреве и повышает хрупкость при охлаждении;
- сера приводит к образованию микротрещин.
Низкоуглеродистая сталь
В состав сплава могут попадать и другие примеси.
Легированная сталь
Для обретения сплавом требуемых свойств при плавке в него добавляют полезные присадки, или легирующие элементы, чаще всего металлы, такие, как алюминий, молибден, хром, марганец, никель, ванадий и другие. Свойства сплава меняются при этом весьма существенно: сплав приобретает стойкость к коррозии, особую прочность, высокую ковкость, повышенную или пониженную электропроводность и т.д.Сплав с такими добавками называют легированной сталью. По процентному содержанию легирующих присадок они делятся на три группы:
- высоколегированные – свыше 11;
- среднелегированные – от 4 до 11;
- низколегированные – менее 4.
По области применения стальные сплавы делятся на:
- инструментальные — высокопрочные сплавы применяются для изготовления инструментов, штампов, фрез, сверл и резцов;
- конструкционные – применяются для производства корпусов и узлов транспортных средств, станков, строительных конструкций;
- специальные. В эту группу включают сплавы с повышенной стойкостью к кислотной и щелочной среде, радиации, нержавеющие сплавы, электроматериалы и др.
Легированая сталь
Некоторые присадки и виды обработки повышают плотность материала, а другие – снижают, например:
| Метод обработки или присадка | Изменение плотности |
| углерод | снижается |
| хром, алюминий, марганец | снижается |
| кобальт, вольфрам, медь | растет |
| волочение | растет в пределах трех процентов |
Удельный вес металла. Таблица плотности металлов и сплавов
Все металлы обладают определенными физико-механическими свойствами, которые, собственно говоря, и определяют их удельный вес. Чтобы определить, насколько тот или иной сплав черной или нержавеющий стали подходит для производства рассчитывается удельный вес металлопроката.
Все металлические изделия, имеющие одинаковый объем, но произведенные из различных металлов, к примеру, из железа, латуни или алюминия, имеют различную массу, которая находится в прямой зависимости от его объема. Иными словами, отношение объема сплава к его массе – удельная плотность (кг/м3), является постоянной величиной, которая будет характерной для данного вещества.
Плотность сплава рассчитывается по специальной формуле и имеет прямое отношение к расчету удельного веса металла.
В таблице даны плотности металлов цветных и черного железа.
Таблица разделена на группы металлов и сплавов, где под каждым наименованием обозначена марка по ГОСТ и соответствующая ей плотность в г/см3 в зависимости от температуры плавления.
Для определения физического значения удельной плотности в кг/м3 нужно табличную величину в г/см3 умножить на 1000. Например, так можно узнать какова плотность железа – 7850 кг/м3.
Наиболее типичным черным металлом является железо. Значение плотности – 7,85 г/см3 можно считать удельным весом черного металла на основе железа.
− легкие – магний, алюминий;
− благородные металлы (драгоценные) – платина, золото, серебро и полублагородная медь;
− легкоплавкие металлы – цинк, олово, свинец.
| Наименование металла, обозначение | Атомный вес | Температура плавления, °C | Удельный вес, г/куб.см |
| Цинк Zn (Zinc) | 65,37 | 419,5 | 7,13 |
| Алюминий Al (Aluminium) | 26,9815 | 659 | 2,69808 |
| Свинец Pb (Lead) | 207,19 | 327,4 | 11,337 |
| Олово Sn (Tin) | 118,69 | 231,9 | 7,29 |
| Медь Cu (Сopper) | 63,54 | 1083 | 8,96 |
| Титан Ti (Titanium) | 47,90 | 1668 | 4,505 |
| Никель Ni (Nickel) | 58,71 | 1455 | 8,91 |
| Магний Mg (Magnesium) | 24 | 650 | 1,74 |
| Ванадий V (Vanadium) | 6 | 1900 | 6,11 |
| Вольфрам W (Wolframium) | 184 | 3422 | 19,3 |
| Хром Cr (Chromium) | 51,996 | 1765 | 7,19 |
| Молибден Mo (Molybdaenum) | 92 | 2622 | 10,22 |
| Серебро Ag (Argentum) | 107,9 | 1000 | 10,5 |
| Тантал Ta (Tantal) | 180 | 3269 | 16,65 |
| Железо Fe (Iron) | 55,85 | 1535 | 7,85 |
| Золото Au (Aurum) | 197 | 1095 | 19,32 |
| Платина Pt (Platina) | 194,8 | 1760 | 21,45 |
Таблица удельного веса сплавов металлов
Удельный вес металлов определяют чаще всего в лабораторных условиях, но в чистом виде они весьма редко применяются в строительстве. Значительно чаще находится применение сплавам цветных металлов и сплавам черных металлов, которые по удельному весу подразделяют на легкие и тяжелые.
Легкие сплавы активно используются современной промышленностью, из-за их высокой прочности и хороших высокотемпературных механических свойств. Основными металлами подобных сплавов выступают титан, алюминий, магний и бериллий. Но сплавы, созданные на основе магния и алюминия, не могут использоваться в агрессивных средах и в условиях высокой температуры.
В основе тяжелых сплавов лежит медь, олово, цинк, свинец. Среди тяжелых сплавов во многих сферах промышленности применяют бронзу (сплав меди с алюминием, сплав меди с оловом, марганцем или железом) и латунь (сплав цинка и меди). Из этих марок сплавов производятся архитектурные детали и санитарно-техническая арматура.
Ниже в справочной таблице приведены основные качественные характеристики и удельный вес наиболее распространенных сплавов металлов. В перечне представлены данные по плотности основных сплавов металлов при температуре среды 20°C.
| Список сплавов металлов | Плотность сплавов(кг/м3) |
| Адмиралтейская латунь – Admiralty Brass (30% цинка, и 1% олова) | 8525 |
| Алюминиевая бронза – Aluminum Bronze (3-10% алюминия) | 7700 – 8700 |
| Баббит – Antifriction metal | 9130 -10600 |
| Бериллиевая бронза (бериллиевая медь) – Beryllium Copper | 8100 – 8250 |
| Дельта металл – Delta metal | 8600 |
| Желтая латунь – Yellow Brass | 8470 |
| Фосфористые бронзы – Bronze – phosphorous | 8780 – 8920 |
| Обычные бронзы – Bronze (8-14% Sn) | 7400 – 8900 |
| Инконель – Inconel | 8497 |
| Инкалой – Incoloy | 8027 |
| Ковкий чугун – Wrought Iron | 7750 |
| Красная латунь (мало цинка) – Red Brass | 8746 |
| Латунь, литье – Brass – casting | 8400 – 8700 |
| Латунь, прокат – Brass – rolled and drawn | 8430 – 8730 |
Технические показатели сплавов металлов
Наиболее распространенными сплавами на основе меди считаются латунь и бронза. Их состав формируется также из других элементов:
- цинка;
- никеля;
- олова;
- висмута.
Все сплавы различаются между собой структурой. Наличие олова в составе позволяет делать бронзовые сплавы отменного качества. В более дешевые сплавы входит никель либо цинк. Производимые материалы на основе Cuprum  обладают следующими характеристиками:
обладают следующими характеристиками:
- высокая пластичность и износостойкость;
- электропроводность;
- устойчивость к агрессивной среде;
- низкий коэффициент трения.
Сплавы на основе меди находят широкое применение в промышленном производстве. Из них производят посуду, ювелирные украшения, электропровода и системы отопления. Материалы с Cuprum часто используют для декорирования фасадной части домов, изготовления композиций. Высокая устойчивость и пластичность являются основными качествами для применения материала.
Металлы и их плотность
Металлические материалы представляют собой твердые вещества при комнатной температуре и атмосферном давлении (исключением является лишь ртуть). Они обладают высокой пластичностью, электро- и теплопроводностью и имеют характерный блеск в отполированном состоянии поверхности. Многие свойства металлов связаны с наличием у них упорядоченной кристаллической решетки, в узлах которой сидят положительные ионные остовы, связанные друг с другом с помощью отрицательного электронного газа.
Что касается плотности металлов, то она изменяется в широких пределах. Так, наименее плотными являются щелочные легкие металлы, такие как литий, калий или натрий. Например, плотность лития составляет 534 кг/м3, что практически в два раза меньше аналогичной величины для воды. Это означает, что пластинки из лития, калия и натрия не будут тонуть в воде. С другой стороны, такие переходные металлы, как рений, осмий, иридий, платина и золото, обладают огромной плотностью, которая в 20 и более раз превышает ρ воды.
Ниже приведена таблица плотности металлов. Все значения соответствуют комнатной температуре в г/см3. Если эти значения умножить на 1 000, то мы получим ρ в кг/м3.
Почему существуют металлы с высокой плотностью и с низким ее значением? Дело в том, что значение ρ для каждого конкретного случая определяется двумя основными факторами:
Особенностью кристаллической решетки металла. Если эта решетка будет содержать атомы в максимально плотной упаковке, тогда макроскопическая его плотность будет выше. Самой плотной упаковкой обладают ГЦК и ГПУ решетки.
Физическими свойствами атома металла. Чем больше его масса и чем меньше радиус, тем выше значение ρ. Этот фактор объясняет, почему металлами с высокой плотностью являются химические элементы с большим номером в периодической таблице.
Альтернативная классификация
Разнообразие видов вторичного металлического сырья, а также способов его переработки выдвигает требования категоризации металлолома по тем или иным признакам. Основная стандартизация отходов металлов сведена в ГОСТ, однако существует альтернативная классификация вторичного чермета, производимая по таким признакам:
происхождение;
необходимость, а также тип предварительной подготовки;
направление применения в металлургическом производстве.
При таком подходе важными характеристиками лома становятся не только его вид, качество
Непосредственное внимание необходимо уделять физическим параметрам, включая степень однородности, плотность
Соответственно физическому состоянию металлолома различают стандартную плотность лома черных металлов и насыпную. Последний вариант характерен, например, для стружки и определяется отношением массы отходов металлического вторичного сырья, к занимаемому ими объему.
Свойства
Главным достоинством медной проволоки является ее малое удельное сопротивление. Именно поэтому она активно применяется в электроэнергетике и конструкциях различных электроприборов. Получение проводов существенно облегчает высокая пластичность металла. Качественную медь несложно обрабатывать в режиме высокой точности. Формулу сплава подбирают в различных случаях индивидуально, отталкиваясь от того, какие целевые свойства должны быть достигнуты. Температура плавления чистой меди составляет 1083 градуса по Цельсию или же 1356 градусов по Кельвину. А плотность этого металла составляет 2,07 г на 1 см3. Потому просчитать массу по сечению несложно:
- при толщине 1,5 кв. мм. – 0,0133 кг на 1 м3;
- при сечении 4 кв. мм. – 0,035 кг на 1 м3;
- при сечении 6 кв. мм. – 0,053 кг на 1 м3.


Пластичность:
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними.
Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0,003 мм, которую используют для золочения изделий. Однако не все металлы пластичны. Проволока из цинка или олова хрустит при сгибании; марганец и висмут при деформации вообще почти не сгибаются, а сразу ломаются.
Пластичность зависит и от чистоты металла. Так, очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым. Некоторые металлы, такие, как золото, серебро, свинец, алюминий, осмий, могут срастаться между собой, но на это могут уйти десятки лет.
Особенности никеля и его сплавов
Никель имеет особые характеристики, которые высоко ценятся в промышленном производстве. Благодаря хорошей пластичности, из него легко получать изделия различной формы с помощью технологий холодной и горячей деформации. При этом свариваемость сплавов на никелевой основе находится на высоком уровне.
Стоит отметить высокую стойкость никеля к агрессивной среде щелочных растворов и других химических веществ. Он не вступает в реакцию с кислородом в нормальных условиях, даже при нагреве до температуры 800 градусов благодаря жаростойкости. Его плотность может варьироваться в зависимости от наличия в составе таких газов, как кислород, окись углерода и водорода, а также серы, железа, кремния, свинца, марганца, цинка и других элементов.
Никель отлично взаимодействует в сплавах с большинством металлов благодаря свойству активной катализации. С его помощью можно значительно улучшить или изменить свойства различных материалов, что позволяет получать ценнейшие изделия. На сегодняшний день известно более 3000 сплавов с применением этого элемента.
Но кроме сплавов на его основе, никель может применяться в чистом виде. Очень часто его используют для формирования антикоррозийной защиты. Для ее нанесения обычно используют метод гальванизации или плакирования, который используют при защите железа и стали. С помощью такого метода можно получить материал, практически не уступающий по свойствам чистому металлу, при этом удается значительно удешевить изделия. Используя метод гальванизации, защищают алюминий, чугун, магний и цинк.
Несмотря на свою высокую стоимость, из чистого металла очень часто производят различные приборы и аппараты, а также тигли для металлургии. В химической промышленности используют цистерны, резервуары и трубки из этого металла, которые применяются для хранения и перегрузки пищевых продуктов, щелочных и иных веществ.
В процессе производства водорода его применяют в качестве конденсаторов. Также следует отметить медицинскую сферу, где очень часто применяются никелевые инструменты и приборы.
Также следует отметить, что он особо популярен в сфере строения радиоприборов и телевизионных гаджетов. Его можно считать незаменимым в атомной сфере, так как без его использования невозможно получить высокоточные аппараты дистанционного управления.
Гранулированный никель широко применяется в качестве катализатора множества химических реакций с участием углеводородов, спиртов и альдегидов. Им обычно заменяют платину и палладий, так как свойства этого гранулированного металла не уступают вышеуказанным, при этом он дешевле.
Порошкообразный никель также используется как элемент фильтрующих аппаратов, необходимых для очистки газов, топливных жидкостей и других веществ, производимых химической промышленностью.
Также подобный порошок отлично подходит для производства сплавов, поэтому очень часто именно такому физическому состоянию металла отдают предпочтение в металлургии.
В металлургической промышленности множество видов стали, особенно конструкционных, производится с никелем в качестве легирующего компонента. При этом нет разницы, будь то магнитные, немагнитные, или жаропрочные никелевые сплавы.
Наиболее часто никель используют в сплавах вместе с медью. Это позволяет получить материал, обладающий повышенными свойствами устойчивости к агрессивной среде, особенно щелочной, морской воде и повышенной влажности. Именно поэтому их широко применяют в медицине, морском деле, химической и пищевой промышленности.
Сплавы серебра и никеля имеют интересные свойства: при сплавлении только этих двух элементов получается неустойчивый материал, характерный ломкостью и предрасположенностью к появлению трещин. Но при использовании этих сплавов в качестве легирующих элементов в сплавах на основе других металлов, можно значительно повысить устойчивость к коррозии.

Чистый никель
В ювелирном деле очень часто используют его сплав с золотом. Из него получают прочные ювелирные изделия, для которых характерен белый цвет. Но у некоторых людей наблюдается аллергическая реакция на такие изделия.
Также никель в чистом виде и в составе сплавов часто используется для производства нагревательных элементов и приборов.
Физические свойства металлов
Твёрдость
Все металлы (кроме ртути и, условно, франция) при нормальных условиях находятся в твёрдом состоянии, однако обладают различной твёрдостью. Ниже в таблице приводится твёрдость некоторых металлов по шкале Мооса.
| Твёрдость | Металл |
|---|---|
| 0.2 | Цезий |
| 0.3 | Рубидий |
| 0.4 | Калий |
| 0.5 | Натрий |
| 0.6 | Литий |
| 1.2 | Индий |
| 1.2 | Таллий |
| 1.25 | Барий |
| 1.5 | Стронций |
| 1.5 | Галлий |
| 1.5 | Олово |
| 1.5 | Свинец |
| 1.5 | Ртуть(тв.) |
| 1.75 | Кальций |
| 2.0 | Кадмий |
| 2.25 | Висмут |
| 2.5 | Магний |
| 2.5 | Цинк |
| 2.5 | Лантан |
| 2.5 | Серебро |
| 2.5 | Золото |
| 2.59 | Иттрий |
| 2.75 | Алюминий |
| 3.0 | Медь |
| 3.0 | Сурьма |
| 3.0 | Торий |
| 3.17 | Скандий |
| 3.5 | Платина |
| 3.75 | Кобальт |
| 3.75 | Палладий |
| 3.75 | Цирконий |
| 4.0 | Железо |
| 4.0 | Никель |
| 4.0 | Гафний |
| 4.0 | Марганец |
| 4.5 | Ванадий |
| 4.5 | Молибден |
| 4.5 | Родий |
| 4.5 | Титан |
| 4.75 | Ниобий |
| 5.0 | Иридий |
| 5.0 | Рутений |
| 5.0 | Тантал |
| 5.0 | Технеций |
| 5.0 | Хром |
| 5.5 | Бериллий |
| 5.5 | Осмий |
| 5.5 | Рений |
| 6.0 | Вольфрам |
| 6.0 | β-Уран |
Температура плавления
Температуры плавления чистых металлов лежат в диапазоне от −39 °C (ртуть) до 3410 °C (вольфрам). Температура плавления большинства металлов (за исключением щелочных) высока, однако некоторые металлы, например, олово и свинец, могут расплавиться на обычной электрической или газовой плите.
Плотность
В зависимости от плотности, металлы делят на лёгкие (плотность 0,53 ÷ 5 г/см³) и тяжёлые (5 ÷ 22,5 г/см³). Самым лёгким металлом является литий (плотность 0,53 г/см³). Самый тяжёлый металл в настоящее время назвать невозможно, так как плотности осмия и иридия — двух самых тяжёлых металлов — почти равны (около 22,6 г/см³ — ровно в два раза выше плотности свинца), а вычислить их точную плотность крайне сложно: для этого нужно полностью очистить металлы, ведь любые примеси снижают их плотность.
Пластичность
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними. Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0,003 мм, которую используют для золочения изделий. Однако не все металлы пластичны. Проволока из цинка или олова хрустит при сгибании; марганец и висмут при деформации вообще почти не сгибаются, а сразу ломаются. Пластичность зависит и от чистоты металла; так, очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым. Некоторые металлы, такие, как золото, серебро, свинец, алюминий, осмий, могут срастаться между собой, но на это могут уйти десятки лет.
Электропроводность
Все металлы хорошо проводят электрический ток; это обусловлено наличием в их кристаллических решётках подвижных электронов, перемещающихся под действием электрического поля. Серебро, медь и алюминий имеют наибольшую электропроводность; по этой причине последние два металла чаще всего используют в качестве материала для проводов. Очень высокую электропроводность имеет также натрий, в экспериментальной аппаратуре известны попытки применения натриевых токопроводов в форме тонкостенных труб из нержавеющей стали, заполненных натрием. Благодаря малому удельному весу натрия, при равном сопротивлении натриевые «провода» получаются значительно легче медных и даже несколько легче алюминиевых.
Теплопроводность
Высокая теплопроводность металлов также зависит от подвижности свободных электронов. Поэтому ряд теплопроводностей похож на ряд электропроводностей, и лучшим проводником тепла, как и электричества, является серебро. Натрий также находит применение как хороший проводник тепла; широко известно, например, применение натрия в клапанах автомобильных двигателей для улучшения их охлаждения.
Наименьшая теплопроводность — у висмута и ртути.
Цвет
Цвет у большинства металлов примерно одинаковый — светло-серый с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
Сферы применения сплавов меди
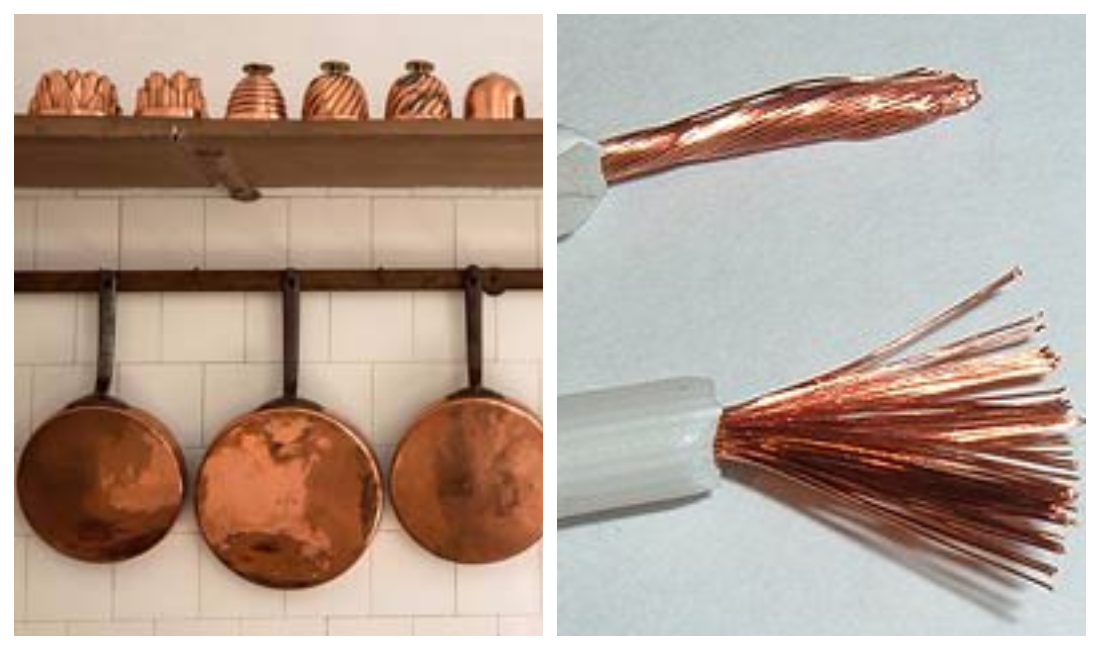 От проводов до посуды – широкое применение сплавов меди.
От проводов до посуды – широкое применение сплавов меди.
- Благодаря физическим и механическим свойствам химический элемент применяется в разных отраслях производства. Медь является составной частью электропроводов, систем отопления и охлаждения.
- Медные провода используются в бытовых электрических двигателях и трансформаторах. При этом применяют чистый металл, присутствие примесей снижает проводимость.
- Металл является отличным материалом для создания строительных конструкций, труб, кровельных покрытий. Механическая прочность, устойчивость, пригодность к механической обработке позволяют создавать бесшовные трубы, используемые в системах водоснабжения.
- На стенках проката не образуется налет солей, растворенных в воде. Такие трубопроводы используются в энергетике и судостроении для транспортировки пара и жидкости. В тонкодисперсной форме металл используется в лазерах, работающих на парах меди.
- Сплавы, в состав которых входит медь, применяются в ювелирном производстве. Сочетание золота и меди повышает прочность изделия, устойчивость к деформации.
- Оксиды химического элемента являются основой для получения сверхпроводников, а чистый металл применяется для производства батарей и гальванических элементов.
- Медь используют в качестве материала для изготовления композиций, назначенных для декорирования фасадов домов. Очень часто возле входа в кафе можно встретить скульптуры, изготовленные из бронзы. Причина использования материала — высокая пластичность и устойчивость.
- Изделия из бронзы отличаются устойчивостью к воздействию морской воды, поэтому ее используют как материал для изготовления разных приспособлений для навигации и эксплуатации судов.
- Латунь в чистом виде уязвима к воздействию агрессивной среды. Для того чтобы добиться устойчивости к реагентам, сплав подвергают легированию другими металлами: алюминием, оловом или свинцом.
Подведем итоги
Меня постоянно спрашивают, как выяснить, настоящее серебро или подделка. Прочитав этот обзор, вы узнали, дорогие читатели, что серебро чрезвычайно теплопроводно, поэтому можно воспользоваться простым методом – опустить его в кипяток (если изделие без камней). Оно моментально нагреется, но остынет так же очень быстро в отличие от подделки.
Читать также: Замена аккумуляторов в шуруповерте интерскол
Это важно знать, так как покупать стоит только настоящие, качественные изделия. Серебряные сплавы востребованы как в ювелирной отрасли, так и в медицине из-за противомикробного эффекта, в нанотехнологиях, в микроэлектронике (не забываем, что этот металл – прекрасный проводник)
Это природный исчерпаемый ресурс, обладающий массой особенных свойств. Делитесь этой информацией в соцсетях, подписывайтесь на нас, чтобы узнать новые и полезные сведения. До скорых встреч!
Серебряные сплавы востребованы как в ювелирной отрасли, так и в медицине из-за противомикробного эффекта, в нанотехнологиях, в микроэлектронике (не забываем, что этот металл – прекрасный проводник). Это природный исчерпаемый ресурс, обладающий массой особенных свойств. Делитесь этой информацией в соцсетях, подписывайтесь на нас, чтобы узнать новые и полезные сведения. До скорых встреч!
| Плотность | |
| ρ = m V ho =>> | |
| Размерность | L −3 M |
| Единицы измерения | |
| СИ | кг/м³ |
| СГС | г/см³ |
| Примечания | |
| скалярная величина |
Пло́тность
— скалярная физическая величина, определяемая как отношение массы тела к занимаемому этим телом объёму .
Для обозначения плотности обычно используется греческая буква ρ (происхождение обозначения подлежит уточнению), иногда используются также латинские буквы D
иd (от лат. densitas «плотность»).
Более точное определение плотности требует уточнение формулировки:
- Средняя плотность тела — отношение массы тела к его объёму. Для однородного тела она также называется простоплотностью тела .
- Плотность вещества — это плотность однородного или равномерно неоднородного тела, состоящего из этого вещества.
- Плотность тела в точке — это предел отношения массы малой части тела ( Δ m ), содержащей эту точку, к объёму этой малой части ( Δ V ), когда этот объём стремится к нулю , или, записывая кратко, lim Δ V → 0 Δ m / Δ V >. При таком предельном переходе необходимо помнить, что на атомарном уровне любое тело неоднородно, поэтому необходимо остановиться на объёме, соответствующем используемой физической модели.
Поскольку масса в теле может быть распределена неравномерно, более адекватная модель определяет плотность в каждой точке тела как производную массы по объёму. Если учитывать точечные массы, то плотность можно определить как меру, либо как производную Радона — Никодима по отношению к некоторой опорной мере.